Anforderungen an Hersteller von Biosimilars
Die Produktion von Biosimilars stellt an Hersteller große Herausforderungen und erfordert eine ständige Qualitätskontrolle des Produktes.
5 Fakten über die Herstellung von Biosimilars
- Biosimilars werden durch sehr aufwändige biotechnologische Verfahren in lebenden Zellen hergestellt.
- Bei der Herstellung von Biosimilars werden in der Regel keine menschlichen Zellen eingesetzt.
- Hersteller von Biosimilars müssen bei der Produktion hohe Anforderungen erfüllen.
- Es ist nicht möglich, eine hundertprozentige Kopie eines Biologikums herzustellen.
- Für die Zulassung von Biosimilars bestehen strenge Zulassungskriterien, die von der europäischen Zulassungsbehörde EMA vorgegeben werden.
Biosimilars – Hohe Anforderungen an Hersteller
Biosimilars werden durch sehr aufwändige und teilweise empfindliche biotechnologische Prozesse in lebenden Zellen, wie z. B. in Bakterien- oder Hefezellen, hergestellt. Diese komplexen Produktionsprozesse stellen sehr hohe Anforderungen an die Hersteller von Biosimilars und erfordern ein großes Fachwissen der Firmen.
Grundsätzlich ist es für den Hersteller eines Biosimilars nicht möglich, eine hundertprozentige Reproduktion des Original-Medikaments herzustellen. Hierfür gibt es zwei Gründe: Zum einen sind die genauen Schritte des Herstellungsprozesses ein gut gehütetes Geheimnis des ehemaligen Patentinhabers. Jeder Hersteller entwickelt daher seine eigenen, neuen Herstellungsverfahren und verwendet außerdem seine eigenen, einzigartigen Zelllinien. Zum anderen kommt es bei der Herstellung eines so komplexen Produktes wie eines Biosimilars immer zu Abweichungen – und das nicht nur zwischen Original-Arzneimittel und Biosimilar, sondern sogar zwischen verschiedenen Produktionschargen des Originals, aber auch beim Biosimilar. Diese Abweichungen dürfen aber keinesfalls die Wirksamkeit und Verträglichkeit des Biosimilars beeinträchtigen. Daher gibt es für alle Parameter eines Wirkstoffes festgelegte Ober- und Untergrenzen, die eingehalten werden müssen. Innerhalb dieser Grenzwerte muss sich das Biosimilar immer bewegen.
Damit eine Einhaltung der Grenzwerte und damit eine gleichbleibende Qualität der Biosimilars möglich ist, gibt es einige Faktoren bei der Herstellung, die vorab genau festgelegt werden und innerhalb des Produktionsprozesses fortlaufend durch den Hersteller überwacht werden müssen. Zu diesen Faktoren gehören beispielsweise:
- Auswahl der Zelllinie, die für die Herstellung genutzt wird
- Technischer Aufbau der Produktionsanlage, in der die Herstellung mit Billionen von Zellen stattfindet
- Zusammensetzung und Eigenschaften der Nährmedien, in denen sich die Zellen vermehren
- Temperaturverhältnisse während der Produktion, um eine gleichbleibende Qualität und konstante Eigenschaften des Wirkstoffs zu gewährleisten
- Ablauf des anschließenden Aufreinigungsprozesses, der die Reinheit des Wirkstoffes gewährleistet
Welche Zellen verwenden Hersteller von Biosimilars?
Biosimilars sind Proteine (Eiweiße), die in lebenden Zellen gebildet werden. Für ihre Produktion verwenden die Hersteller von Biosimilars in der Regel aber nicht die Zellen, in denen die Wirkstoffe in der Natur vorkommen, sprich menschliche Zellen. Stattdessen handelt es sich bei Biosimilars in den meisten Fällen um sogenannte ektopische Moleküle, die in einem fremden Organismus oder einer fremden Zelle hergestellt werden. Dies hat einen sicherheitsrelevanten Grund: Würden aus menschlichen Zellen isolierte Proteine als Wirkstoff verwendet werden, bestünde die Gefahr einer Verunreinigung mit menschlichen Krankheitserregern. Daher werden bei der Herstellung von Biosimilars Bakterien-, Hefe- oder Zellen anderer Säugetiere eingesetzt. In der späteren Anwendung des Biosimilars bringt dieses Vorgehen deutliche Vorteile und mehr Sicherheit für den Patienten.
Damit fremde Zellen überhaupt in der Lage sind ein menschliches Protein zu produzieren, müssen sie vorab mit Methoden der Gentechnologie in einem höchst komplexen Vorgang „umprogrammiert“ werden. Hierfür ist es zuerst notwendig, das Gen in der menschlichen DNA, dem Träger des Erbgutes, zu identifizieren, das die Bauanleitung für dieses bestimmte Eiweiß trägt. Diese Anleitung besteht aus einem einzigartigen genetischen Code, der universell ist. Dies bedeutet, dass ein Gen, das beim Menschen für ein bestimmtes Protein kodiert, dies auch in allen anderen Organismen tut. Deshalb wird das entsprechende Gen mit Hilfe der Gentechnik in eine Bakterien-, Pilz- oder Säugetierzelle eingeschleust. Dieses Verfahren wird Gentransfer genannt. Danach ist die Zelle in der Lage, ein Protein zu produzieren, das im menschlichen Körper wirksam werden kann. Für die Produktion von Biosimilars werden diese Zellen dann zunächst in einer Zellkultur gezüchtet und anschließend in kleinen Mengen in flüssigem Stickstoff bei -196°C eingefroren.
Übrigens: Die am häufigsten eingesetzten Säugetierzellen sind die sogenannten Chinese Hamster-Ovary-Zellen. Diese entstammen alle ursprünglich aus dem Eierstock eines einzigen Hamsters und wurden bereits 1957 an der Universität Denver gewonnen.
Aktuell verwenden Hersteller von Biosimilars nur wenige verschiedene Zelllinien in der Produktion. Jede Zelllinie hat ihre Vorteile, aber auch Nachteile. Während die Herstellung von Biosimilars in Bakterien oder Hefen vergleichsweise günstig und in Bezug auf Verunreinigungen mit Viren sehr sicher ist, ist die anschließende Aufreinigung des Produktes, die die Reinheit des Wirkstoffes gewährleisten soll, meist sehr kompliziert. Einige Wirkstoffe lassen sich andererseits nur in Säugetier-Zelllinien herstellen, die wiederum bei der Vermehrung der Zellen sehr anspruchsvoll und kostenintensiv sind. Außerdem steigen bei zunehmender genetischer Ähnlichkeit zu menschlichen Zellen die Anforderungen, um Verunreinigungen durch Krankheitserreger auszuschließen.
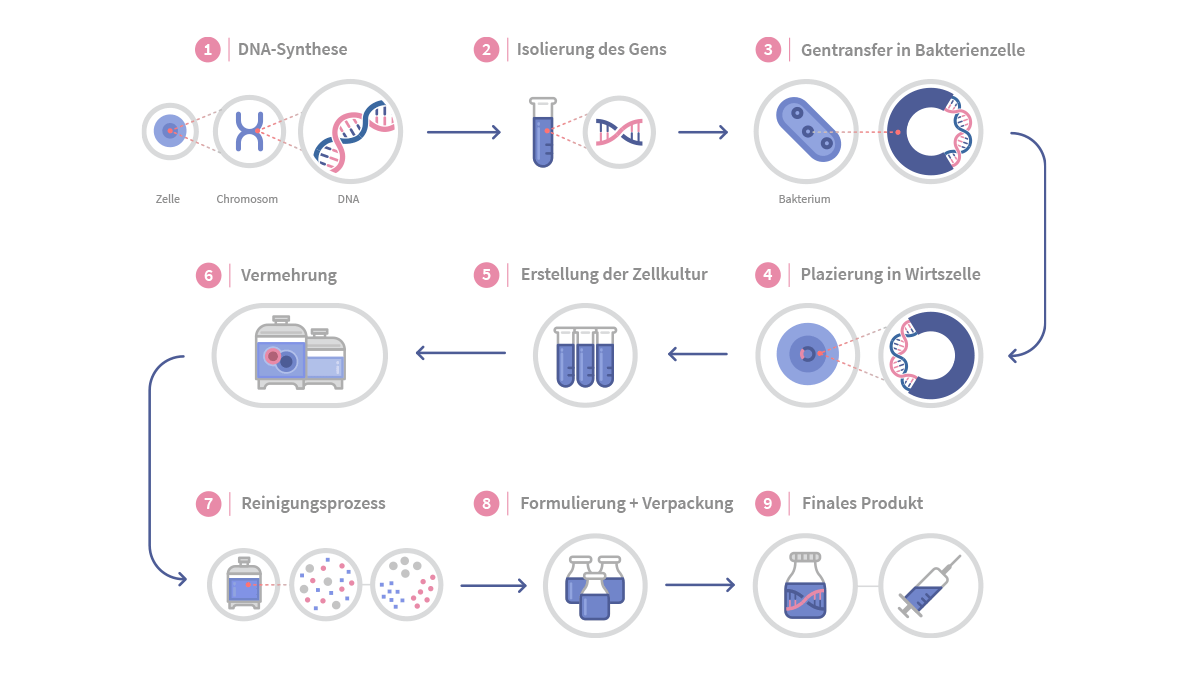
Wie erfolgt die Herstellung von Biosimilars?
Sobald die Produktion der Biosimilars starten kann, wird eine entsprechende Menge rekombinanter Zellen aufgetaut und in eine Nährsubstanz in einem geschlossenen Tank, dem Fermenter, gegeben. Dort können sie sich unter keimfreien, sterilen Bedingungen vermehren, bis sie eine bestimmte Zellzahl erreicht haben. In einem Fermenter mit 20.000 Litern leben beispielsweise am Ende bis zu 60 Billionen Zellen. Dabei reicht es nicht, die Zellen einfach vor sich hin wachsen zu lassen. Die Vermehrung erfordert viel wissenschaftliches Fachwissen, bis die optimale Temperatur, Nährstoffzusammensetzung oder Rührgeschwindigkeit gefunden ist. Außerdem kann es mehrere Monate dauern, bis ausreichend Zellen angewachsen sind, um das Biosimilar in einer genügend großen Menge aus ihnen gewinnen zu können.
Auch der anschließende Reinigungsprozess ist sehr komplex. Zum einen dürfen dabei die Wirksamkeit und Stabilität des Biosimilars nicht beeinträchtigt werden, zum anderen müssen aber auch alle Zellreste entfernt werden, da diese später die Verträglichkeit des Wirkstoffes beeinflussen könnten. Nur wenige Hersteller in Deutschland und Europa beherrschen diese Verfahren, sodass sich die Produktion auf wenige Marktführer aufteilt.
Welche Rolle spielen Biosimilars in der medizinischen Versorgung?
Fast in jedem Land der Europäischen Union sind Biosimilars zugelassen und werden in der Therapie verschiedener Erkrankungen verwendet. Da sie kostengünstiger als das Original-Arzneimittel hergestellt werden können, ist die Verschreibung für Ärzt:innen ökonomischer. Auf diese Weise ermöglichen sie mehr Patient:innen den Zugang zu einer Therapie mit effizienten, modernen Wirkstoffen. Da in den nächsten Jahren die Patente zahlreicher weiterer Biologika auslaufen, können weitere Biosimilars auf den Markt gebracht werden. Es besteht also in diesem Bereich ein großes Potenzial, weitere Kosten im Gesundheitssystem einzusparen.
So können Biosimilars einen erheblichen Beitrag leisten, nämlich mehr Patient:innen eine zusätzliche moderne Behandlungsoption zu bieten.